LITFULO (Ritlecitinib) de Pfizer es el único tratamiento para la alopecia areata severa aprobado para pacientes a partir de los 12 años.
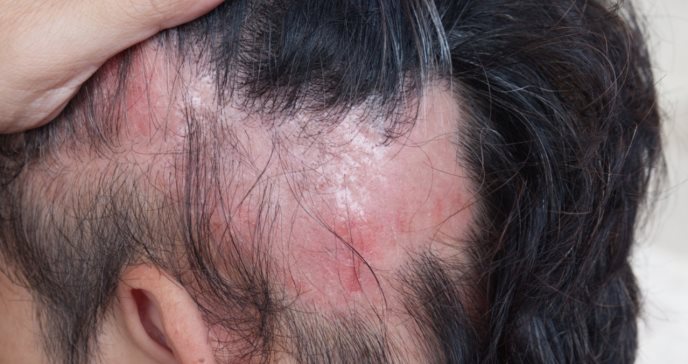
Pfizer Inc. anunció que la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) ha aprobado LITFULO ™ (ritlecitinib), un tratamiento oral de una vez al día, para personas mayores de 12 años con alopecia areata severa.
La dosis recomendada aprobada para LITFULO es de 50 mg, siendo el primer y único tratamiento aprobado por la FDA para adolescentes mayores de 12 años que padecen la enfermedad.
"Aunque algunos pacientes pueden comenzar a desarrollar síntomas de alopecia areata a cualquier edad, la mayoría de las personas empiezan a mostrar signos en la adolescencia, en los veinte o los treinta años", afirmó la Dra. Brittany Craiglow, profesora asociada adjunta del departamento de Dermatología en la Escuela de Medicina de Yale.
"LITFULO es una opción de tratamiento especialmente importante para los pacientes más jóvenes con pérdida considerable de cabello, quienes a menudo luchan con una enfermedad tan visible".
Cabe mencionar que LITFULO es un inhibidor de cinasa que inhibe la cinasa de Janus 3 (JAK3) y la familia de las cinasas tirosinas expresadas en el carcinoma hepatocelular (TEC).
"LITFULO es un importante avance en el tratamiento de alopecia areata, una enfermedad autoinmune que previamente no tenía opciones aprobadas por la FDA para adolescentes y que disponía con opciones limitadas para adultos" indicó Angela Hwang, directora comercial y presidenta de Global Biopharmaceuticals Business, Pfizer.
La aprobación de la FDA se basó en los resultados de los ensayos clínicos en alopecia areata. El ensayo ALLEGRO Fase 2b/3, en el que participaron 718 pacientes con un 50 % o más de pérdida de cabello, según el Severity of Alopecia Tool (SALT), evaluó la eficacia y seguridad de LITFULO en 118 centros en 18 países.
En este estudio central, el 23 % de los pacientes tratados con LITFULO 50 mg tenían una cobertura del 80 % o más del cuero cabelludo luego de seis meses comparado con el 1.6 % con placebo.
La eficacia y seguridad de LITFULO fueron concordantes entre adolescentes (de 12 a 17 años) y adultos (de 18 años en adelante). Por otro lado, los efectos secundarios más comunes notificados en al menos un 4 % de los pacientes con LITFULO incluyeron dolor de cabeza (10.8 %), diarrea (10 %), acné (6.2 %), erupción cutánea (5.4 %) y urticaria (4.6 %).
Al respecto, Nicole Friedland, presidenta y directora General de la National Alopecia Areata Foundation (NAAF), mencionó que, "las personas que viven con alopecia areata a menudo son incomprendidos y su experiencia se trivializa con ´es solo pelo´. Sin embargo, se trata de una enfermedad autoinmune grave que puede tener repercusiones negativas considerables más allá de los síntomas físicos".
"Creemos que la aprobación de LITFULO es un avance significativo para el tratamiento de la alopecia areata, en particular para los adolescentes. Es emocionante ver qué hay más tratamientos aprobados por la FDA disponibles para esta comunidad", añadió.