El diagnóstico de necrosis por radiación requirió excluir recidiva tumoral mediante espectroscopia, perfusión cerebral y PET-TAC, y fue establecido por un equipo conjunto de oncología y neurología.
El paciente, un varón de 49 años con antecedentes de tabaquismo y cáncer testicular tratado previamente, presentó un cuadro de tres meses de evolución caracterizado por fiebre intermitente, cefalea holocraneana progresiva y aumento de volumen cervical izquierdo.
El examen físico reveló múltiples adenopatías cervicales firmes y fijas, siendo la mayor de ellas localizada en región yugulodigástrica izquierda con 3.7 cm de diámetro. La nasofibroscopia mostró una lesión exofítica en pared lateral de nasofaringe izquierda.
El estudio histopatológico de la biopsia nasofaríngea demostró un carcinoma escamocelular indiferenciado con marcada infiltración linfocitaria. La inmunohistoquímica fue positiva para CK5/6 y p40, con índice de proliferación Ki-67 del 70%. La PET-TAC de cuerpo completo evidenció hipercaptación en nasofaringe (SUVmax 12.3) y en múltiples ganglios cervicales bilaterales (SUVmax 8.7-10.2), sin evidencia de metástasis a distancia.
El estudio de extensión incluyó resonancia magnética de cráneo que descartó invasión de base de cráneo en el momento del diagnóstico.
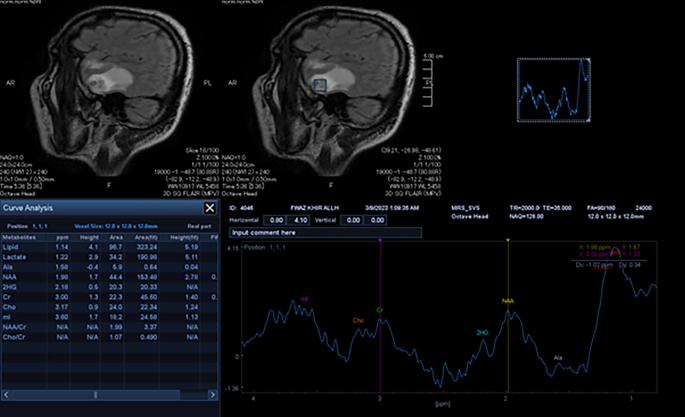
Una imagen del espectro de efectos a corto plazo de la prensa que muestra un pico alto de lactato con colina normal, excluyendo alta celularidad o destrucción celular como se ve en lesiones neoplásicas y sugiriendo necrosis debido a hipoxia (niveles altos de lactato en la espectroscopia de resonancia magnética)
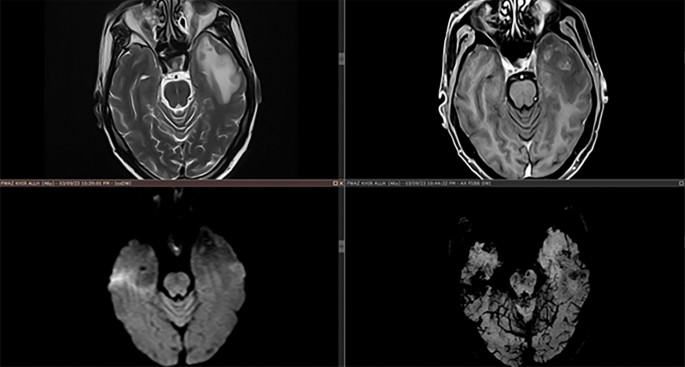
Una imagen de resonancia magnética del cerebro que muestra cuatro cuartos: el cuarto superior izquierdo es una imagen ponderada en T2, el cuarto superior derecho es una imagen ponderada en T1 con contraste, el cuarto inferior izquierdo es una imagen de resonancia magnética ponderada por difusión, el cuarto inferior derecho es una imagen ponderada por susceptibilidad.
El tratamiento consistió en quimioterapia de inducción con tres ciclos de TPF (docetaxel 75 mg/m² día 1, cisplatino 75 mg/m² día 1, 5-FU 750 mg/m²/día días 1-5) cada 21 días, seguido de quimiorradioterapia concurrente. La planificación radioterápica mediante IMRT administró 66 Gy en 33 fracciones a volumen tumoral primario y ganglios afectados, con dosis de 54 Gy a áreas de riesgo. La dosimetría mostró que el lóbulo temporal izquierdo recibió una dosis media de 45 Gy (V60 < 15%, V65 < 5%).
La evaluación postratamiento mostró respuesta completa tanto clínica como radiológica. La PET-TAC de control a los 3 meses demostró normalización metabólica completa (SUVmax < 2.5 en lecho tumoral).
Sin embargo, cinco meses después el paciente desarrolló deterioro cognitivo progresivo con afasia nominal y desorientación temporoespacial. La evaluación neuropsicológica objetivó déficits en memoria episódica (percentil 15 en test de Rey) y fluencia verbal (percentil 20).
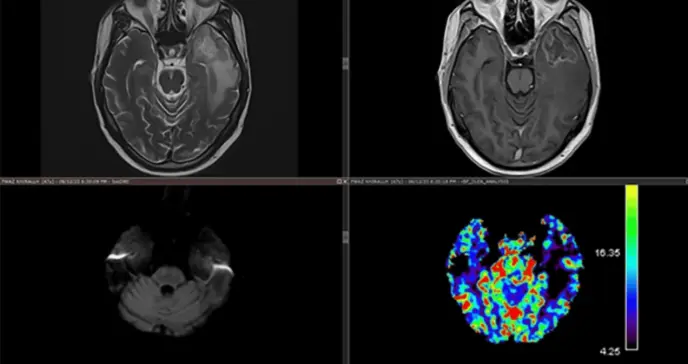
La resonancia magnética cerebral con secuencias avanzadas mostró una lesión en lóbulo temporal izquierdo de 18x13 mm con características típicas de necrosis por radiación: hiperseñal en T2/FLAIR, realce anular en T1 con gadolinio, restricción en difusión y espectroscopia con elevación de lactato (2.3 ppm) y reducción de NAA (1.8 ppm). El estudio de perfusión no mostró hipervascularización, descartando recidiva tumoral. El EEG demostró actividad delta focal temporal izquierda sin descargas epileptiformes.
El comité de tumores de cabeza y cuello, en conjunto con neurología, estableció el diagnóstico de necrosis cerebral tardía grado 3 según CTCAE v5.0. El tratamiento incluyó:
1. Medidas sintomáticas: levetiracetam 1000 mg/día, memantina 20 mg/día y terapia neurocognitiva intensiva
2. Terapia específica: inicio de bevacizumab intravenoso 7.5 mg/kg cada 3 semanas durante 4 ciclos
3. Control evolutivo con RM mensuales y evaluación neuropsicológica seriada
Evolución clínica y pronóstico
A los 6 meses del diagnóstico de necrosis, se observó mejoría radiológica con reducción del 40% en el volumen lesional y mejoría subjetiva en las funciones cognitivas (incremento al percentil 35 en memoria y 40 en fluencia verbal).
Sin embargo, persistían secuelas neuropsicológicas que limitaban su reinserción laboral. El pronóstico a largo plazo se consideró reservado, con riesgo de deterioro progresivo y necesidad de seguimiento indefinido.
Este caso (Jlailati, A., et al), ilustra una complicación grave de la radioterapia en región craneofacial. La necrosis cerebral tardía ocurre típicamente 6 meses a 3 años postratamiento, con incidencia del 3-5% en pacientes que reciben >60 Gy.
Los factores de riesgo incluyen dosis por fracción >2 Gy, volumen cerebral irradiado, quimioterapia concurrente y susceptibilidad individual. El diagnóstico diferencial debe incluir recidiva tumoral, metástasis cerebral y procesos desmielinizantes, requiriendo técnicas avanzadas de imagen para su diferenciación.
Perspectivas terapéuticas actuales
El manejo óptimo combina medidas sintomáticas, farmacológicas (corticoides, bevacizumab) y rehabilitación.
Estudios recientes sugieren que la oxigenoterapia hiperbárica podría tener un rol en estadios precoces, aunque su disponibilidad es limitada. La prevención mediante técnicas de radioterapia de última generación (protonterapia, IMRT con reducción de márgenes) representa la estrategia más prometedora para minimizar esta complicación devastadora.